山西专版2022中考化学复习方案题型突破09科学探究题试题
此题为判断题(对,错)。
A、NaOH固体
B、40%NaOH溶液
C、30%NaOH溶液
D、50%NaOH溶液
此题为判断题(对,错)。
配制好的NaOH需贮存于( )中。
A.棕色橡皮塞试剂瓶
B.白色橡皮塞试剂瓶
C.白色磨口塞试剂瓶
D.塑料瓶
下列化学试剂的理化性能表述不正确的是()
A.NaOH片状或粒状固体,强碱性
B.H2SO4液体比重大,强酸性
C.KmnO4黄色固体,强酸
D.H2C2O4白色固体,弱酸
题型突破(九)科学探究题类型一 有关变质问题的探究1.2022山西百校联考二某校兴趣小组同学在配制NaOH溶液后,忘记盖上NaOH固体的试剂瓶盖,一段时间后,发现瓶中原片状固体上出现了大量的白色粉末。同学们对这些白色粉末产生了浓厚的兴趣并进行研究。问题一:这瓶NaOH固体是否变质?猜想与假设NaOH固体没有变质;NaOH固体变质。作出猜想的依据是(用化学方程式表示)。进行实验实验步骤实验现象实验结论取少量固体于试管中参加适量水溶解,向其中参加过量稀盐酸 NaOH固体变质分析思考反响后的溶液中存在的离子主要有。问题二:如果变质,是全部变质还是局部变质呢?进行实验实验步骤实验现象实验结论取少量固体于试管中并参加适量水溶解,向其中参加过量的溶液,静置取上层溶液,滴加无色酚酞溶液并观察有白色沉淀生成 NaOH固体局部变质反思与评价氢氧化钠应保存。2.2022山西百校联考二实验室中有一个已经用完的氢氧化钙溶液试剂瓶,化学研究小组发现其内壁上有白色固体。这种白色固体中有哪些成分?小组同学利用实验室中的试剂展开了如下的探究。进行猜想小红认为可能是氢氧化钙,原因是溶液中的水蒸发后溶质析出。小明认为可能是碳酸钙,原因是(写出发生变化的化学方程式)。你认为还可能是。实验验证为了验证各自的猜想,小组的同学进行了如下的实验操作。(1)小明同学取少量白色固体,向其中参加稀盐酸,振荡,发现有气泡产生。小明认为他的猜想正确,小红认为这个结论不正确,原因是。(2)为了正确获取结论,小组同学经过讨论,用以下的实验完成了探究。实验操作实验现象实验结论取少量白色固体,向其中参加一定量的蒸馏水,搅拌, 你的猜想正确反思交流小组对用完后的氢氧化钙溶液试剂瓶提出了如下的处理建议:a.用后应及时清洗,试剂瓶已经洗净的标准是。b.通过上面的分析,在保存大量氢氧化钙溶液时,应保存。c.小组同学想用另一种试剂检验碳酸钙的存在,可选择的试剂是。3.2022山西百校联考二 在实验室,小明发现一瓶没有瓶塞的 NaOH 固体,对其是否变质以及变质程度产生了兴趣。 于是小明和他的小伙伴们作出了以下猜想,并进行如下实验探究。提出问题 这瓶 NaOH 固体样品的成分是什么呢?作出猜想 猜想1:只含NaOH;猜想2:只含 Na2CO3;猜想3:。讨论交流 NaOH变质的原因是(用化学方程式表示)。实验探究(1)取少量样品于试管中,参加足量稀盐酸,有气泡产生,说明猜想不成立。(2)进一步探究过程如下: 图T9-1根据上述探究过程答复:操作a为;参加过量 BaCl2 溶液的作用是;小明同学说还可以用适量 Ba(OH)2 溶液代替过量 BaCl2 溶液,你认为(填“行或“不行),原因是;检验猜想成立,还可以选用的试剂是(指示剂除外)。实验反思 实验室里,NaOH固体的保存方法是。类型二 无明显现象反响的实验探究4.2022山西百校联考四学习碱的化学性质后,我们知道碱能与某些非金属氧化物反响。老师将二氧化碳通入氢氧化钠溶液中,但未看到明显现象,同学们分小组设计实验证明反响发生。下面是某一小组的交流过程。设计方案 图T9-2交流讨论经讨论,同学们认为上述两个方案都不正确。甲同学的方案中,写出在实施过程中观察到的现象,该方案不能证明反响发生的理由是。进行实验随后,同学们进行了如下正确的实验:实验步骤实验现象结论取NaOH溶液于试管中,向其中通入CO2,再向其中参加 二氧化碳与氢氧化钠发生反响反思交流请你再写出一个没有明显现象的化学方程式:。经过上述探究活动,同学们认为对于这类无明显现象的反响,想要证明其发生,我们设计实验的思路是。5.2022山西百校联考三化学变化有的伴随明显的现象,有的无明显现象。 某兴趣小组的同学们收集、整理了一些无明显现象的化学反响:二氧化碳与水反响;二氧化碳与氢氧化钠反响;盐酸与氢氧化钠反响。实验探究 为了证明这些化学反响的发生,各小组设计了如下方案:组别实验操作实验现象实验结论组证明 CO2 可与 H2O 反响组无色酚酞溶液变红证明 CO2 可与 NaOH反响组溶液由红色变成无色证明盐酸可与NaOH反响得出结论 同学们一致认为,只有组的设计方案是合理的,写出其反响的化学方程式:。评价反思 (1)组设计的方案不严谨,请你说明理由:。(2)同学们对组的设计方案进行改良,能充分证明二氧化碳与氢氧化钠发生了化学反响。实验方案实验现象取二氧化碳通入氢氧化钠溶液后的液体少许于试管中,滴加足量的(3)同学们又重新设计了如下方案,也能证明二氧化碳与氢氧化钠发生了反响。实验操作实验装置实验现象分别向两个收集满 CO2 气体的软塑料瓶中参加约13体积的水和 NaOH 溶液,立即旋紧瓶盖,振荡 归纳总结 同学们总结得出:证明无明显现象的化学反响发生的方法有;。6.2022山西适应性训练九年级某化学小组的同学们学习“中和反响后,在实验室里他们将一定量的氢氧化钠溶液与稀硫酸混合,如图T9-3甲所示,其反响的化学方程式为;同学们发现该反响没有明显的现象,进行了如下实验探究。图T9-3提出问题1如何验证该反响已经发生?进行实验同学们分别取图甲中B中溶液进行两个实验,结果如图乙所示。反思评价你认为上述实验能验证反响已经发生的是实验,请选择上述任一实验从微观角度分析其正确或错误的理由。提出问题2图甲B中溶液中溶质的成分有哪些?进行实验实验操作实验现象结论取B中的少量溶液于试管中参加观察到B中溶液的溶质是Na2SO4和H2SO4经思考,同学们认为用另一种不同类别的试剂,也能到达相同的目的。拓展延伸将C中试管中的物质静置,上层清液中一定含有的溶质是。类型三 反响后溶液成分的探究7.2022龙东某实验小组将澄清石灰水和碳酸钾溶液混合,充分反响后过滤,得到了滤液M,同学们对滤液M中溶质的成分进行了探究,探究过程如下:猜想与假设含有KOH;含有;含有KOH、K2CO3;含有KOH、K2CO3和Ca(OH)2。设计与实验(1)大家认为猜想一定不正确,其原因是。(2)甲同学取滤液M样品,向其中参加足量的,不产生气泡,那么猜想不正确。(3)乙同学依据甲同学的实验结论继续实验,记录如下:实验操作现象结论取一定量滤液M于试管中,参加溶液猜想成立相关反响的化学方程式为。交流与反思假设将滤液M直接倒入下水道,对环境造成的影响是。8.2022哈尔滨工业采用电解氯化钠溶液制备烧碱。某同学取电解后的溶液进行如下探究:提出问题电解后的溶液中的溶质是什么?猜想假设(1)NaOH、NaCl;(2)NaOH。实验探究取电解后的溶液,进行如下实验:图T9-4收集证据实验1的反响现象为(1),实验2发生反响的化学方程式为(2)。实验结论电解后的溶液中的溶质是(3)。表达交流实验中滴加酚酞溶液的作用是(4)。在滴加过量稀硝酸的过程中,图T9-5中表示的是(5)(填符号),表示的是(6)(填符号)。图T9-5总结规律通过探究还可认识到:上述实验1和实验2的反响都
【试题】已知一包白色粉末可能含有的成分是CuS04、CaC03、BaCl2、Na2S04、NaOH。为探究其组成,进行以下实验:
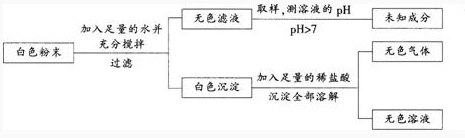
根据以上实验,可以判断白色粉末中,一定含有的物质是什么?一定没有的物质是什么?
【考试结果】很多学生提交了如下答案:肯定含有的物质是CaC03、NaOH,一定没有的物质是CuS04、BaCl2、Na2S04。
根据上述信息,回答下列问题:
(1)本题中白色粉末中一定含有的物质是什么?一定没有的物质是什么?
(2)试对学生答题错误的原因进行分析和诊断。
(3)为了进一步确定该白色粉末中物质的真实组成,还需要做的实验及其现象是什么?
(1)白色粉末中一定含有的物质是CaC03、NaOH,一定没有的物质是CuS04。
(2)产生错误的原因:学生知道BaCl2和Na2S04反应会生成不溶于稀盐酸的沉淀,而认为白色粉末中一定没有BaCl2和Na2S04。但学生忽略了固体粉末中可能含有BaCl2或Na2S04中的一种,因而只从上述实验并不能确定是否含有BaCl2或Na2S04,一定没有的物质也并不包括BaCl2和Na2S04。
(3)①取未知成分溶液少许,加入氯化钡溶液.若有白色沉淀,则白色粉末中含有硫酸钠.若没有沉淀,则白色粉末中不含硫酸钠;②取未知成分溶液少许。加入硫酸钠溶液,若有白色沉淀,则白色粉末中含有氯化钡,若没有白色沉淀,则白色粉末中不含氯化钡。
配制好的NaOH需贮存于()中。
- A、白色磨口试剂瓶
- B、棕色磨口试剂瓶
- C、白色橡皮塞试剂瓶
- D、大烧杯
正确答案:C
欲配制10%的NaOH溶液500克,需要固体NaOH和水各多少克?
正确答案: 固体NaOH质量为:500×10%=50g
水的质量为:500-50=450g
欲配制10%的NaOH溶液500克,需要固体NaOH和水各多少克?
正确答案: 固体NaOH质量为:500×10%=50g
水的质量为:500-50=450g
有一种白色固体,可能是KI、CaI2、KIO3、BaCl2中的一种或两种的混合物,试根据下述实验判别白色固体的组成。 (1)将白色固体溶于水得到无色溶液; (2)向此溶液加入少量的稀H2SO4后,溶液变黄并有白色沉淀,遇淀粉立即变蓝; (3)向蓝色溶液加入NaOH到碱性后,蓝色消失而白色并未消失。
正确答案:白色固体的组成为:CaI2,KIO3的混合物
