问答题什么叫化学反应速率?浓度、压强和温度对化学平衡和化学反应速率的影响?
题目
问答题
什么叫化学反应速率?浓度、压强和温度对化学平衡和化学反应速率的影响?
相似考题
参考答案和解析
正确答案:
在其他条件不变的情况下,增加反应物浓度或减少生成物浓度,化学平衡向正反应方向移动;增加生成物浓度或者减少反应物浓度,化学平衡向着逆反应的方向移动。增大反应物的浓度,也可以增大化学反应速率。
对有气体参与的反应,若反应前后气体分子数不相等,则在等温下,增大总压强,平衡向气体分子数减少的方向移动;减压,则平衡向气体分子数增加的方向移动。增大压强,也可以增大化学反应速率。
温度的影响与反应的热效应有关,升高温度,使平衡向吸热方向移动;降低温度,使平衡向放热方向移动。升高温度,也可以增大化学反应速率。
对有气体参与的反应,若反应前后气体分子数不相等,则在等温下,增大总压强,平衡向气体分子数减少的方向移动;减压,则平衡向气体分子数增加的方向移动。增大压强,也可以增大化学反应速率。
温度的影响与反应的热效应有关,升高温度,使平衡向吸热方向移动;降低温度,使平衡向放热方向移动。升高温度,也可以增大化学反应速率。
解析:
暂无解析
更多“什么叫化学反应速率?浓度、压强和温度对化学平衡和化学反应速率的影响?”相关问题
-
第1题:
什么叫化学反应速率影响化学反应速率的主要因素(内因和外因)有哪些。参考答案:化学反应的速率用单位时间内反应物浓度的减少或生成物浓度的增加来表示,它着眼于物质的种类和质量的变化。影响化学反应速率的因素分为内因和外因两个方面。内因是指反应物本身的性质,如金属钠与冷水剧烈反应,而镁和沸水仅能微弱反应。影响化学反应速率的决定因素是内因。外因是指外界条件如浓度、压强、温度、催化剂等。改变了这些条件,可以改变化学反应速率,其根本原因是改变了单位体积内活化分子数目,也就改变了分子间发生有效碰撞的机会,从而改变了化学反应速率。其他条件:除上述四种常见的反应条件外,还有光、超声波、激光、放射线、电磁波等均可改变化学反应速率。
-
第2题:
下列说法不正确的是( )A.增大压强,活化分子百分数不变,化学反应速率增大
B.升高温度,活化分子百分数增大,化学反应速率增大
C.增大反应物浓度,活化分子百分数增大,化学反应速率增大
D.使用催化剂,活化分子百分数增大,化学反应速率增大答案:C解析:A.增大压强,增大单位体积内活化分子个数,从而增大有效碰撞几率,导致反应速率增大,故A正确;
B.升高温度,增大活化分子百分数,从而增大有效碰撞几率,导致反应速率增大,故B正确;
C.增大反应物浓度,增大单位体积内活化分子个数,从而增大有效碰撞几率,反应速率增大,故C错误;
D.使用催化剂,增大活化分子百分数,从而增大有效碰撞几率,反应速率增大,故D正确;
故选C. -
第3题:
影响化学反应的速率的因素有浓度、温度、()。
正确答案:催化剂 -
第4题:
影响化学反应速率的决定性因素是()
- A、反应物的种类和性质
- B、浓度
- C、压力,温度
- D、催化剂
正确答案:A -
第5题:
化学反应的活化能愈大,下列什么因素对化学反应速率的影响较大()
- A、反应物的浓度
- B、压力
- C、反应的级数
- D、温度
正确答案:D -
第6题:
温度对反应速率的影响()。
- A、反应速率常数随温度升高而很快增大
- B、温度升高只影响正向反应速率
- C、阿累尼乌斯公式反映了浓度对反应速率的影响
- D、化学反应速率常数不随温度变化
正确答案:A -
第7题:
影响化学反应速率的因素有()等。
- A、温度
- B、压强
- C、浓度
- D、催化剂
正确答案:A,B,C,D -
第8题:
什么叫化学反应速率?浓度、压强和温度对化学平衡和化学反应速率的影响?
正确答案: 在其他条件不变的情况下,增加反应物浓度或减少生成物浓度,化学平衡向正反应方向移动;增加生成物浓度或者减少反应物浓度,化学平衡向着逆反应的方向移动。增大反应物的浓度,也可以增大化学反应速率。
对有气体参与的反应,若反应前后气体分子数不相等,则在等温下,增大总压强,平衡向气体分子数减少的方向移动;减压,则平衡向气体分子数增加的方向移动。增大压强,也可以增大化学反应速率。
温度的影响与反应的热效应有关,升高温度,使平衡向吸热方向移动;降低温度,使平衡向放热方向移动。升高温度,也可以增大化学反应速率。 -
第9题:
浓度、温度、催化剂是决定化学反应速率的外因。
正确答案:正确 -
第10题:
判断题浓度、温度、催化剂是决定化学反应速率的外因。A对
B错
正确答案: 对解析: 暂无解析 -
第11题:
填空题影响化学反应速率的主要因素有浓度、压强、温度和()。正确答案: 催化剂解析: 暂无解析 -
第12题:
问答题试述浓度、压强和温度如何影响化学平衡和化学反应速率?正确答案: 在其他条件不变的情况下,增加反应物浓度或减少生成物浓度,化学平衡向正反应方向移动;增加生成物浓度或者减少反应物浓度,化学平衡向着逆反应的方向移动。增大反应物的浓度,也可以增大化学反应速率。
对有气体参与的反应,若反应前后气体分子数不相等,则在等温下,增大总压强,平衡向气体分子数减少的方向移动;减压,则平衡向气体分子数增加的方向移动。增大压强,也可以增大化学反应速率。
温度的影响与反应的热效应有关,升高温度,使平衡向吸热方向移动;降低温度,使平衡向放热方向移动。升高温度,也可以增大化学反应速率。解析: 暂无解析 -
第13题:
填表说明改变条件对化学反应速率和化学平衡移动的影响. 答案:解析:
答案:解析:
-
第14题:
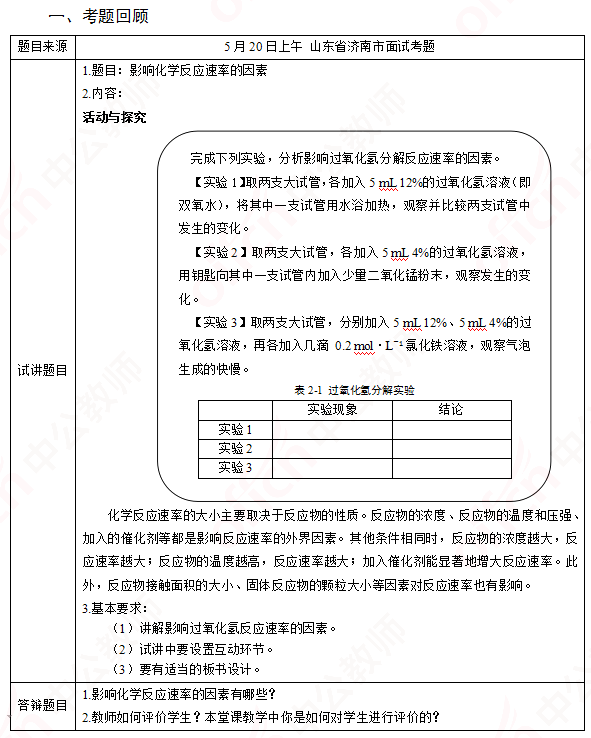
高中化学《影响化学反应速率的因素》
二、考题解析
【教学过程】
(一)图片导入
【展示图片】面包的标签。请学生观察保质期。
【提出问题】根据生活常识知道在不同温度条件下,面包的保质期长短不同,那么温度是如何影响化学反应的快慢?除了温度还有哪些因素会影响化学反应的快慢呢?
(二)探究新知
【展示图片】请学生回忆初中学过的不同金属单质(镁、铝、锌、铁)与稀盐酸的反应。
【提出问题】在外界条件相同的情况下,不同的金属单质与稀盐酸反应,它们的快慢并不相同,这说明了什么?
【学生回答,教师总结】决定化学反应快慢的主要因素是反应物本身的性质。
【教师引导】那么外界条件对化学反应速率的影响是怎样的呢?能不能通过实验验证温度、催化剂、浓度对化学反应速率的影响呢?请同学们利用实验台上的药品、仪器等设计实验。接下来同学们以分好的实验小组为单位,讨论一下如何设计实验,7分钟之后请小组代表回答设计的方案。
(学生小组讨论环节)
【学生回答】①温度对化学反应速率的影响:控制其他外界条件相同,观察相同浓度的双氧水在不同温度下分解的反应速率;
②催化剂对化学反应速率的影响:控制其他外界条件相同,观察相同浓度的双氧水分别加入催化剂、不加入催化剂的反应速率;
③浓度对化学反应速率的影响:观察不同浓度的双氧水在相同条件的反应速率。
【教师引导】在做实验的时候注意控制好外界条件,各个小组按照自己小组设计的实验方案来进行实验,在实验的时候注意观察实验现象,并由此判断外界条件对化学反应速率的影响是怎样的。
(学生分组实验环节,教师巡视指导。)
【学生回答,小组总结】①温度对化学反应速率的影响:温度影响化学反应的速率,温度越高化学反应速率越快,反之越慢;
②催化剂对化学反应速率的影响:催化剂影响化学反应的速率,催化剂可以大大加快反应的速率;
③浓度对化学反应速率的影响:浓度影响化学反应的速率,浓度越大反应速率越大。
【提出问题】下列事实中,什么因素影响了化学反应的速率?
(1)铁矿石炼铁时要粉碎成矿粒。
(2)实验室进行化学反应时,常常把一些固体物质溶于水配成溶液再进行反应。
(3)工业合成氨,通常在2×107~5×107Pa的压强下进行。
【小组回答】
①反应物表面积:有固体参加的反应,固体的表面积越大,化学反应速率越快。
②反应物状态:通常气相或液相反应比固相反应的反应速率大。
③压强:对于有气体参加的反应,改变压强将使气体的体积发生改变,即相应地改变气体的浓度。
(三)拓展提升
【教师提问】在超市,为什么有很多的食品放置在冰柜当中,有什么作用?
【学生回答】通过降低温度有助于减慢化学反应速率,防止食品变质。
(四)小结作业
小结:总结影响化学反应速率的因素。
作业:调查生活生产中改变外界因素调节反应速率的实例,并用化学知识解释。

【答辩题目解析】
1.影响化学反应速率的因素有哪些?
2.教师如何评价学生?本堂课教学中你是如何对学生进行评价的?答案:解析:1、影响化学反应的速率分为内因和外因。内因是影响化学反应速率的本质也就是物质本身的性质,外因有反应物的浓度、温度、压强、催化剂。另外反应物的状态,比如块状还是粉末状,有没有搅拌等也会影响化学反应的速率。
2、新课改理念要求教师注重对学生的情感、态度、价值观等方面进行综合评价。“评价”是学校教育教学活动中的一个重要环节。学校要建立评价学生全面发展的指标体系,不仅要关注学生的学业成绩,而且要注重发展和发现学生多方面的潜能和特长,如学生的道德品质、学习的愿望和能力、交流与合作、个性与情感以及创新意识和实践能力等。要采用灵活多样、具有开放性的评价方法,要关注过程性评价,帮助学生认识自我、建立自信,激发其内在的发展动力,使学生全面发展健康成长。本节课通过启发式的提问,引导学生思考,对于思考速度稍慢的同学我会耐心指导,在小组讨论中,我也会下去巡视,时时关注学生的讨论情况,并及时纠正和引导。 -
第15题:
影响化学反应速率的因素主要有浓度、温度、()。
正确答案:催化剂 -
第16题:
试述浓度、压强和温度如何影响化学平衡和化学反应速率?
正确答案: 在其他条件不变的情况下,增加反应物浓度或减少生成物浓度,化学平衡向正反应方向移动;增加生成物浓度或者减少反应物浓度,化学平衡向着逆反应的方向移动。增大反应物的浓度,也可以增大化学反应速率。
对有气体参与的反应,若反应前后气体分子数不相等,则在等温下,增大总压强,平衡向气体分子数减少的方向移动;减压,则平衡向气体分子数增加的方向移动。增大压强,也可以增大化学反应速率。
温度的影响与反应的热效应有关,升高温度,使平衡向吸热方向移动;降低温度,使平衡向放热方向移动。升高温度,也可以增大化学反应速率。 -
第17题:
催化剂可以改变化学反应速率,但是,并不能影响化学平衡。
正确答案:正确 -
第18题:
对于固体物质,影响化学反应速率的因素主要有()。
- A、温度
- B、压强
- C、浓度
- D、催化剂
正确答案:A,D -
第19题:
影响化学反应速率的主要因素有浓度、压强、温度和()。
正确答案:催化剂 -
第20题:
影响化学反应速率的因素有()、()、(),而()对化学反应速率没有影响。
- A、浓度;温度;催化剂;压力
- B、压力;浓度;温度;催化剂
- C、催化剂;压力;浓度;温度
- D、温度;催化剂;压力;浓度
正确答案:A -
第21题:
单选题阿累尼鸟斯定律阐明了()A化学反应速率常数与温度之间的关系
B化学反应速率与反应物浓度的关系
C化学反应的活化能与温度的关系
正确答案: C解析: 暂无解析 -
第22题:
单选题下列条件中,()不会影响化学反应的速率.A浓度
B湿度
C压强
D温度
正确答案: A解析: 暂无解析 -
第23题:
单选题影响化学反应速率的因素有()、()、(),而()对化学反应速率没有影响。A浓度;温度;催化剂;压力
B压力;浓度;温度;催化剂
C催化剂;压力;浓度;温度
D温度;催化剂;压力;浓度
正确答案: B解析: 暂无解析
