单选题标准状况下H2S和O2混合气体100mL,经点燃后反应至完全,所得气体经干燥后,恢复到原来状况时体积为10mL,该10mL气体可能是()A H2S、SO2B O2C H2SD SO3
题目
H2S、SO2
O2
H2S
SO3
相似考题
更多“标准状况下H2S和O2混合气体100mL,经点燃后反应至完全,所得气体经干燥后,恢复到原来状况时体积为10mL,该10m”相关问题
-
第1题:
取0.10ml一氧化碳纯气,用空气稀释至10L,该气体在标准状况下的浓度是A.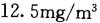
B.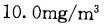
C.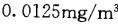
D.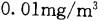
E.未给出配制时的温度和大气压无法计算标准状况下浓度答案:A解析: -
第2题:
将C2H4充入温度为T(120℃)、压力为p的密闭容器中,该容器的容积是可变的,设其初始体积为V。容器中C2H4的体积分数为5.0%,其余为空气。当点燃该混合气体时,发生了C2H4的燃烧反应:C2H4(g)十3O2(g)=2CO2(g)+2H2O(g)。燃烧完全后,让容器恢复到原来的温度和压力,则容器的容积为()
- A、1.15V
- B、1.10V
- C、1.05V
- D、1.00V
正确答案:D -
第3题:
升甲烷、乙烷、甲醛组成的混合气体,完全燃烧后生成15.68升(气体体积均在标准状况下测定),混合气体中乙烷的体积分数为()。
- A、0.2
- B、0.4
- C、0.6
- D、0.8
正确答案:B -
第4题:
设NA为阿伏加德罗常数,下列说法正确的是()。
- A、标准状况下,5.6L四氯化碳含有的分子数为0.25NA
- B、标准状况下,14g氮气含有的核外电子数为5NA
- C、标准状况下,22.4L任意比的氢气和氯气的混合气体中含有的分子总数均为NA
- D、标准状况下,铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为NA
正确答案:C -
第5题:
将20gH2、O2、N2的混合气体点燃,完全反应后生成18gH2O,则剩余的气体不可能是()。
- A、H2和N2
- B、O3和N2
- C、O2和N2
- D、2gN2
正确答案:C -
第6题:
用铝箔包装0.1mol金属钠,用针扎出一些小孔,放入水中,完全反应后,用排水集气法收集产生的气体,则收集到的气体为(标准状况)()。
- A、O2和H2的混合气体
- B、1.12LH2
- C、大于1.12LH2
- D、小于1.12L气体
正确答案:C -
第7题:
已知20℃水的饱和蒸气压为2.34kPa。在20℃,99.3kPa的气压下,用排水集气法收集氮气N2150mL,则纯氮气的分压为()kPa;若该气体在标准状况下经干燥,则此时N2的体积为()mL。
正确答案:97.0;133.8 -
第8题:
已知26℃水的饱和蒸气压为3.33kPa。在26℃,99.99kPa的压力下,在水面上收集氢气(H2)200mL,则纯氢气的分压为()kPa;且氢气的物质的量n为()mol。若该气体在标准状况(101.325kPa、0℃)下经干燥,则此时H2的体积为()mL。
正确答案:96.66;7.78×10-3;174 -
第9题:
单选题设阿佛加德罗常数的符号为NA,标准状况下某种O2和N2的混合气体m克含有b个分子,则n克该混合气体在相同状况下所占体积(L)应是()A22.4nb/NA
B22.4mb/bNA
C22.4nNA/mb
DnbNA/22.4m
正确答案: A解析: 暂无解析 -
第10题:
填空题将20mL乙烷和10mL丙烷混合后,通入装有500mL氧气的容器中,使其完全燃烧;反应后的混合气体经浓硫酸干燥后所剩气体体积是____mL,再经过NaOH溶液,剩余气体体积是____mL(同条件下测定气体体积).正确答案: 450mL,380mL解析:
乙烷和丙烷完全燃烧的化学方程式为:2C2H6+7O2=4CO2+6H2O;C3H8+5O2 =3CO2+4H2O;因此20mL乙烷和10mL丙烷全部反应,消耗掉氧气的体积为70+50=120mL,所以反应过后的混合气体为380mL的氧气和70mL的二氧化碳,所剩气体体积是450mL;经过浓硫酸干燥后,无气体参与反应,全部进入氢氧化钠溶液,而70mL的CO2与NaOH反应生成Na2CO3,所以最后所生的气体为380mL的氧气. -
第11题:
单选题用铝箔包装0.1mol金属钠,用针扎出一些小孔,放入水中,完全反应后,用排水集气法收集产生的气体,则收集到的气体为(标准状况)()。AO2和H2的混合气体
B1.12LH2
C大于1.12LH2
D小于1.12L气体
正确答案: B解析: 暂无解析 -
第12题:
填空题在标准状况下,7g某气体与0.5g氢气所含的分子数相同,则该气体的密度(标准状况下)为____g/L.正确答案: 1.25解析:
0.5g氢气的物质的量为0.25mol,因为7g气体所含分子数与0.5g氢气所含的分子数相同,因此该气体的物质的量也为0.25mol,则该气体的相对分子质量为28,因此在标准状况下,该气体的密度为1.25g/L. -
第13题:
取三个干燥的烧瓶,分别装入标准状况下的干燥氨气、含有二分之一体积空气的氯化氢、二氧化氮和氧气(体积比为4∶1)的混合气体;然后分别做溶解于水的喷泉实验。实验结束后三个烧瓶中所得溶液的物质的量浓度之比为()
- A、2∶1∶2
- B、1∶1∶1
- C、5∶5∶4
- D、7∶7∶4
正确答案:C -
第14题:
氢气和氧气的混合气体共20克,在点燃的条件下,让它们充分反应后,生成9克水,则原混合气体中含有氢气的质量可能是()
- A、8克
- B、12克
- C、11克
- D、无法确定
正确答案:B -
第15题:
在标准状况下,与9.6克氧气体积相等的是()。
- A、标准状况下9.6克二氧化硫
- B、标准状况下0.3摩尔二氧化硫气体
- C、标准状况下9.6克的水
- D、标准状况下0.3摩尔的水
正确答案:B -
第16题:
标准状况下,32g甲烷和6g氢气混合,则混合气体的体积为()升。
- A、112
- B、124
- C、136
- D、148
正确答案:A -
第17题:
2L甲醛气体与xL的氧气混合点燃,甲醛充分反应后,生成的混合气体的体积为aL(气体体积均在120°C,101kPa时测定)。将aL混合气体通过足量的碱石灰后,测得剩余气体的体积为bL。若a-b=3.5,则x的值为()。
- A、2
- B、4
- C、1.75
- D、3.5
正确答案:C -
第18题:
若用排水集气法在295K和压力97.2kPa下收集得氢气850mL,经干燥后氢气的体积为();在标准状况下该干燥气体的体积为()(已知295K时水的饱和蒸气压为2.64kPa)。
正确答案:827mL;734mL -
第19题:
已知23℃水的饱和蒸气压为2.81kPa。在23℃,106.66kPa的压力下,用排水集气法收集氧气(O2)500mL,则纯氧气的分压为()kPa;且氧气的物质的量n为()mol。若该气体在标准状况(101.325kPa、0℃)下经干燥,则此时O2的体积为()mL。
正确答案:103.86;0.0211;473 -
第20题:
一恒容绝热箱中有CH4和O2混合气体,发生化学反应后气体的温度升高、压力增大,则过程的ΔU()0,ΔH()0。
正确答案:=;> -
第21题:
单选题将7.8gNaO和2.7gAl同时放入一定量的水中,充分反应后得到100mL溶液,再向该溶液中缓慢通入HCl气体3.36L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是()。A反应过程中得到3.36L(标准状况)的气体
B反应结束得到3.9g的沉淀
C反应结束得到的溶液中c(Na+)=c(Cl-)+c(OH-)
D反应结束得到的溶液中c(NaCl)=1.0mol·L-1
正确答案: D解析: 暂无解析 -
第22题:
单选题标准状况下,0.56L CH4和C2H4的混合气体通入足量溴水中,溴水增重0.28g(假设C2H4完全被吸收),则乙烯占混合气体体积的( ).A20%
B40%
C60%
D80%
正确答案: A解析:
该混合气体的物质的量为0.025mol,甲烷与溴水不反应,乙烯可以被溴水吸收,由题意可知,吸收的乙烯物质的量为0.01mol,因此,乙烯的体积百分数为40%. -
第23题:
问答题A、B两种气态烃,标准状况下A的密度为1.25g/L,将总质量为4.4g的A、B混合气体4.48L(标准状况下)通入足量的溴的四氯化碳溶液中,充分反应后,溴的四氯化碳溶液的质量增加了2.8g.试求A、B是什么气体?正确答案: A:乙烯;B:甲烷解析:
由于标准状况下烃A的密度为1.25g/L,可知A的相对分子质量M=1.25g/L×22.4L=28g/mol,所以A为乙烯;混合气体体积4.48L,即0.2mol,通入足量的溴的四氯化碳溶液中,乙烯被吸收,因为溴的四氯化碳溶液的质量增加了2.8g,可知原气体中含有0.1mol乙烯,另含有0.1mol B气体,质量为1.6g,即B的相对分子质量为16g/mol,即B为甲烷.
