写出氯化钠溶液和硝酸溶液的化学方程式及离子方程式
题目
写出氯化钠溶液和硝酸溶液的化学方程式及离子方程式
相似考题
更多“写出氯化钠溶液和硝酸溶液的化学方程式及离子方程式”相关问题
-
第1题:
②写出BC“平台”段化学方程式_____________。
正确答案: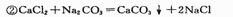
-
第2题:
(10分)CO2是一种常见的氧化物。
(1)CO2能与碱反应,写出它与Ba(OH)2溶液反应的化学方程式:
________________________________________________________________
正确答案:
CO2是一种常见的氧化物。
(1)CO2+ Ba(OH)2== BaCO3↓+ H2O
-
第3题:
下列物质能否发生反应?写出能发生反应的化学方程式。
(1)银与稀盐酸 (2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液
(1)不反应 (2)Zn+CuSO4=ZnSO4+Cu (3)不反应 (4)Al+3AgNO3=Al(NO3)3+3Ag -
第4题:
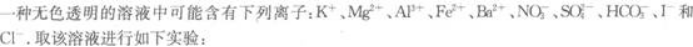
(1)将溶液滴在pH试纸上,试纸显红色.
(2)将少许溶液浓缩后加入铜片和硫酸,有无色气体析出.此气体遇空气则立即变为红棕色.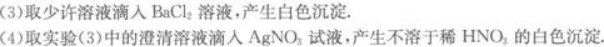
(5)另取少许溶液滴入NaOH溶液,有白色沉淀生成.当NaOH过量时,又有部分白色沉淀溶解.
根据以上现象判断,原溶液中肯定不存在的离子是____________;肯定存在的离子是____________;不能作出判断的离子是____________.写出各步反应的离子方程式____________________________________。答案:解析: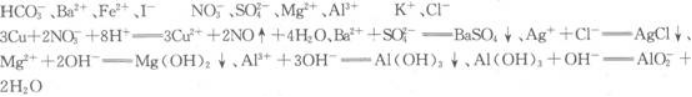
-
第5题:
氯离子的定性检验需用的溶液为()。
- A、硝酸银
- B、石灰水
- C、氯化钠
正确答案:A -
第6题:
有一瓶两种阴离子混合的溶液,加入HCl有浑浊现象,且有刺激性气味产生,加入过量的HCl,再加入BaCl2溶液有白色沉淀产生,问阴离子溶液的组成,并写出反应方程式
正确答案:SO42-,S2O32-
S2O32-+2H+=S↓+SO2↑+H2O
Ba2++SO42-=BaSO4↓ -
第7题:
分别向硝酸银,硝酸铜和硝酸汞溶液中,加入过量的碘化钾溶液,各得到什么产物?写出化学反应方程式
正确答案: Ag++ I-→ AgI↓(黄色)
2Cu2++ 4I-→ 2CuI↓(白色)+ I2(棕色)
Hg2++ 2I-→ HgI2↓(红色)HgI2+ 2I-→ [HgI4]2- -
第8题:
写出铝热焊反应的主要化学方程式。
正确答案: 3FeO+2Al=3Fe+Al2O3Fe2O3+2Al=2Fe+Al2O3
3Fe3O4+8Al=9Fe+4Al2O3 -
第9题:
电位滴定法测定混凝土外加剂氯离子含量,测定时使用的标准溶液为()。
- A、硝酸
- B、硝酸银溶液
- C、氯化钠溶液
- D、盐酸溶液
正确答案:C -
第10题:
往某无色溶液中加入氯化钡溶液,生成不溶于硝酸的白色沉淀,试简答分析该无色溶液中可能含有的化合物类别是什么?并写出有关反应的化学方程式。
正确答案: 无色溶液可能是硫酸或硫酸盐溶液,也可能是硝酸银溶液.BaCl2+H2SO4==BaSO4↓+2HCl
BaCl2+Na2SO4==BaSO4↓+2NaCl
2ANO3+BaCl2==2AgCl↓+Ba(NO3)2 -
第11题:
问答题判断下列反应的产物并写出化学方程式: (1)BF3与过量NaF在酸性水溶液中的反应; (2)BCl3与过量NaCl在酸性水溶液中的反应; (3)BBr3与过量NH(CH3)2在烃类溶剂中的反应。正确答案: (1)BF3是硬Lewis酸,对F-(硬的中强碱)具有较高的亲和力。反应形成配合物:
BF3(g)+ F(aq)=[BF4]-(aq)过量的F-和酸是为了防止pH过高的条件下形成水解产物如[BF3OH] 。
(2)与水解倾向较弱的B—F键不同,其他B—X键极易水解。可以预料BCl3将发生水解而不是与Cl-配位。BCl3(g)+3H2O(l)=B(OH)3(aq)+3HCl(aq)。
(3)NH(CH3)2发生质子转移形成B—N键:BBr3(g)+3NH(CH3)2= B(N(CH3)2)3+3HBr(g),HBr与过量的二甲胺发生质子加合。解析: 暂无解析 -
第12题:
单选题某溶液可能含有Cl-、SO42-,为了检验它们,正确的操作是( ).A先加氯化钠溶液(若有沉淀则滤去),再加硝酸银溶液
B先加硝酸银溶液(若有沉淀则滤去),再加氯化钠溶液
C先加硝酸钡溶液(若有沉淀则滤去),再加硝酸银溶液
D先加硝酸银溶液(若有沉淀则滤去),再加硝酸钡溶液
正确答案: C解析:
可与Cl-产生沉淀的是Ag+,可与SO42-产生沉淀的是Ba2+、Ag+,为了不混淆,则应先加入Ba2+,而后加入Ag+,而加入的溶液中不能含有会对结果产生影响的离子,因此阴离子选择NO3-,故先加硝酸钡溶液(若有沉淀则滤去),再加硝酸银溶液. -
第13题:
(6分)将下列两组中的两种反应物混合,回答下列问题:
(1)根据实验事实完成下表(没有发生反应的,化学方程式一栏“/”)
编号
反应物1
反应物2
现象
化学方程式
1
稀盐酸
氢氧化钾溶液
没有明显现象
2
稀硫酸
氢氧化钡溶液
有白色沉淀生成
3
稀硝酸
澄清石灰水
正确答案:(1)根据实验事实完成下表(没有发生反应的,化学方程式一栏“/”)
编号
反应物1
反应物2
现象
化学方程式
1
稀盐酸
氢氧化钾溶液
没有明显现象
HCl+KOH==KCl+H2O
2
稀硫酸
氢氧化钡溶液
有白色沉淀生成
Ba(OH)2+H2SO4==BaSO4↓+2H2O
3
稀硝酸
澄清石灰水
没有明显现象
2HNO3+Ca(OH)2==Ca(NO3)2+2H2O
-
第14题:
要验证溶液中是否含有SO42-离子,应采用的试剂是()A.酚酞溶液
B.AgNO3溶液及稀硝酸
C.BaCl2溶液及稀硝酸
D.BaCl2溶液
参考答案:C
-
第15题:
根据复分解反应发生的条件,并利用书后附录I所提供的信息,判断下列物质间能否发生复分解反应。如能发生反应,写出反应的化学方程式。
(1)碳酸钠溶液和氯化钙溶液
(2)氢氧化钾溶液和盐酸
(3)氢氧化钠溶液和氯化钾溶液
(4)碳酸钾溶液和盐酸
(5)硫酸铜溶液和氯化钡溶液
① Na2CO3 + CaCl2 = 2NaCl + CaCO3↓ ②KOH + HCl = KCl +H2O ③不能反应 ① K2CO3+2HCl=2KCl+CO2↑+H2O ② CuSO4+BaCl2=BaSO4↓+CuCl2 -
第16题:
做氯离子滴定时,需要硝酸银行溶液和盐酸溶液。()
正确答案:错误 -
第17题:
当含有二价铜离子的溶液与含有CN-离子的溶液相混合时将发生什么变化?若CN-离子过量时,又出现什么现象?为什么?写出有关方程式
正确答案:当Cu2+离子的溶液与含有CN-离子的溶液相混合时,将得到氰化铜的棕黄色沉淀
Cu2++2CN-==Cu(CN)2↓(棕黄色)
CN-过量时,出现紫色,然后马上褪去.这是因为Cu(CN)2在过量CN-
离子中,生成[Cu(CN)4]2-呈现片刻的紫色.[Cu(CN)4]2-在室温下很快失去(CN)2而褪色.
Cu(CN)2+2CN-==〔Cu(CN)4〕2-
2〔Cu(CN)4〕2-==(CN)2↑+2〔Cu(CN)3〕2- -
第18题:
写出高炉中以赤铁矿炼铁的化学方程式及制备CO和除去脉石(SiO2)的化学方程式
正确答案: Fe2O3+3CO======2Fe+3CO2↑
CO2==CO2
CO2+C======2CO
CaCO3======CaO+CO2↑
CaO+SiO2======CaSiO3
(第1,3,4,5个方程式的反应条件是高温) -
第19题:
往10滴0.02mol·L-1铬钾矾溶液中加入5mL2mol·L-1H2SO4,然后加入0.5mol·L-1KMnO4溶液,写出现象及化学方程式
正确答案: 溶液由紫色变为橙色
10Cr3++6MnO4-+11H2O==5Cr2O7+6Mn2++22H+ -
第20题:
写出中变反应的化学方程式:()。
正确答案:CO+H2O→CO2+H2 -
第21题:
KMnO4和NaSO3在强碱性溶液中反应后,溶液呈现()颜色. 写出该反应的离子反应(配平)方程式()。
正确答案:绿;MnO4-+SO32-+2OH-=MnO42-+SO42-+H2O -
第22题:
+3价铁盐跟铁粉在溶液中发生反应能生成亚铁盐,现将生锈的铁粉(足量)放入稀盐酸中,先后观察到哪些现象?写出反应的化学方程式。
正确答案: 先看到溶液变成黄色,然后铁粉表面有气泡生成,最后看到溶液逐渐变成浅绿色:Fe2O3+6HCl===2FeCl3+3H2O
Fe+2HCl===FeCl2+H2↑Fe+2FeCl3====3FeCl2 -
第23题:
单选题电位滴定法测定混凝土外加剂氯离子含量,测定时使用的标准溶液为()。A硝酸
B硝酸银溶液
C氯化钠溶液
D盐酸溶液
正确答案: A解析: 暂无解析
